清华张跃钢教授:镁硫电池中银/氯化银的催化/保护功能可逆转换
【研究背景】
镁金属负极具有成本低廉、化学稳定性高、体积比容量高(3832 mAh·cm-3)等优点,其与硫正极相匹配得到的镁硫电池,有望同时具有极好的安全性和极高的能量密度。然而当前的镁硫电池在放电过程中生成MgS/Mg3S8等不可逆放电产物,导致镁硫电池可逆性差,极化电极电势高,其循环寿命和放电比容量也远低于预期。如何提高镁硫电池中放电产物的可逆性是提升镁硫电池性能的关键问题。
【工作介绍】
清华大学物理系张跃钢教授课题组与美国伯克利国家实验室郭晶华教授团队合作,利用泡沫银作为基底制备了S@Ag正极材料,实现了可100圈以上稳定循环、具有高活性材料利用率(按单质硫质量得到的比容量可达1200 mAh·g-1)的镁硫电池。通过原位X射线衍射(XRD)和原位同步辐射X射线吸收谱(XAS)表征,并结合第一性原理计算,发现了在使用含氯电解液的镁硫电池中Ag表面会随着充放电反应的进行发生Ag和AgCl之间的可逆转化。在充电过程的早期,单质Ag能对MgS的分解提供有效的催化;在充电过程的后期, Ag表面生成AgCl,作为保护层的AgCl有效防止了电化学充电产物S与Ag发生反应,避免了Ag2S的生成。而在放电过程中,在S向MgS转化的同时,AgCl也重新转化为Ag。该文章发表在国际著名期刊Energy Storage Materials上。胥燕博士和赵宇星博士为本文共同第一作者。
【内容表述】
1. DFT计算及电池性能
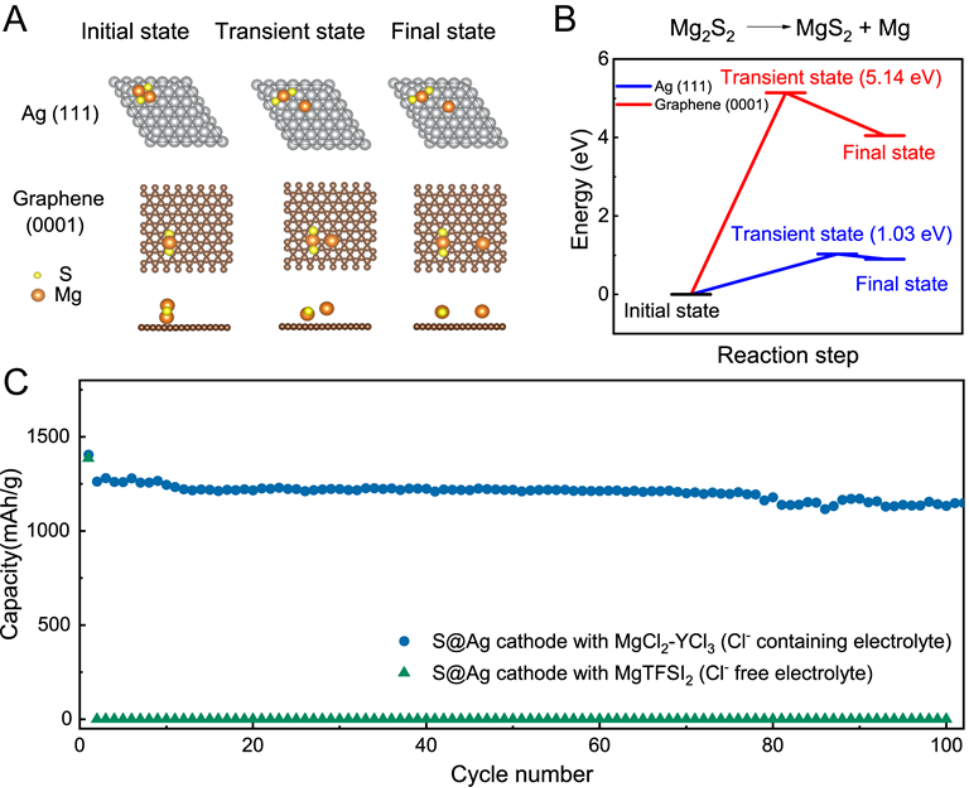
图1(A) MgS在Ag(111)和石墨烯(0001)表面分解过程;DFT计算的在Ag和石墨烯上的分解势垒;(C)Mg/S@Ag电池在含氯和不含氯电解液中的循环性能。
研究者利用DFT的方法分析了MgS在Ag和石墨烯表面的分解势垒。硫化镁的分解是通过Mg2S2簇的初始状态演变为过渡状态来描述的,如图1 A所示。Mg2S2簇其中一个Mg-S键被拉伸至最大值并断裂,最终形成分离的MgS2团簇和Mg原子。DFT计算结果表明MgS在Ag(001)表面的分解势垒为1.03 eV,远低于其在石墨(0001)表面5.14 eV分解势垒,如图1 B所示。图1 C展示了相同的S@Ag电极在含氯的MgCl2-YCl3体系的电解液和不含氯的Mg(TFSI)2体系的电解液中电池循环性能的差异,可以看出在含氯体系的电解液中镁硫电池可以实现100圈循环、比容量为1200 mAh·g-1的性能,而在不含氯的Mg(TFSI)2电解液中电池容量迅速衰减至零。
2. 原位表征
为了研究Ag在镁硫电池中的作用机制,研究者使用原位XRD对S@Ag电极的活化过程和初始充放电过程进行了研究,如图2所示。在活化过程中,初始正极(i-Ag2S)的XRD峰随着放电过程的进行出现了明显的降低,同时在23.7°,27.4°和39.2°出现了新的峰。这些新出现的峰分别对应Ag的(111)、(200)和(220)晶面(图2 A)。这表明在活化过程中i-Ag2S分解生成单质Ag。研究者发现i-Ag2S的分解只发生在初始的活化过程中,在后续的充电过程中,Ag2S的峰并没有出现增加。在第1次充电的末期,研究人员发现了AgCl(220)、(311)和(222)晶面的XRD特征峰的出现(图2A和2B)。这些特征峰在后续的放电过程中会逐步消失,但在后续充电过程中又会逐步生成(图2C和2D)。
研究人员认为S@Ag电极在深度充电的状态下可逆形成的AgCl将有效地保护S不被还原并防止Ag转化为Ag2S,使得单质S可以作为后续放电中的正极材料,而在放电过程中AgCl分解产生Ag可以用于催化后续充电过程中MgS的分解。
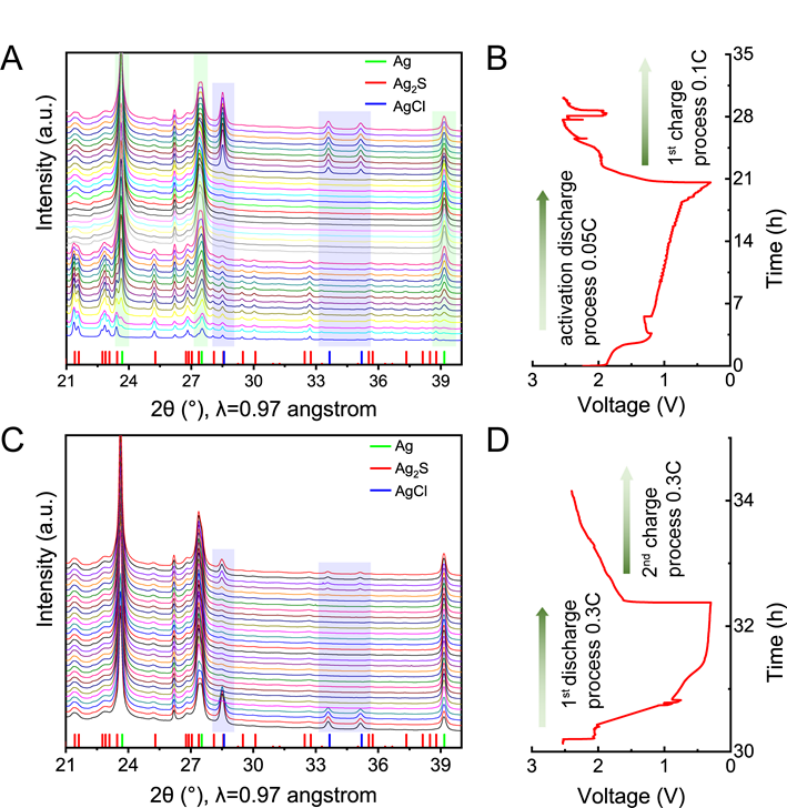
图2 活化过程和第一次充电过程中(A)XRD谱和(B)对应的充放电曲线;第1次放电过程和第2次充电过程中(C)XRD谱和(D)对应的充放电曲线。
由于XRD只对晶相很好的材料有识别作用,而电化学形成的S和MgS产物通常是非晶结构,为了在充放电过程中探测含硫物种的演变,进一步揭示S@Ag电极中Ag的工作机制,研究人员通过原位XAS方法研究S元素化学状态的变化。在S 的K-edge XAS谱中,2472.2 eV、2475.8 eV和2479.0 eV的峰分别对应S0,S2-和TFSI-离子。图3A中黑色的XAS谱线对应初始的i-Ag2S正极。在初始的活化过程中,i-Ag2S的峰逐渐降低,而在2475.8 eV处的MgS特征峰强度逐渐上升(如图3A所示)。这一结果与原位XRD表征结果一致,对应i-Ag2S分解生成MgS和Ag的初始放电活化过程。在后续的充电过程中,MgS的特征峰(2475.8 eV)逐步降低,S0(2472.3 eV)的峰逐步升高。同时,XAS谱显示并没有看到明显的Ag2S的生成。S0和MgS在充电过程中的相对含量变化如图3C所示。
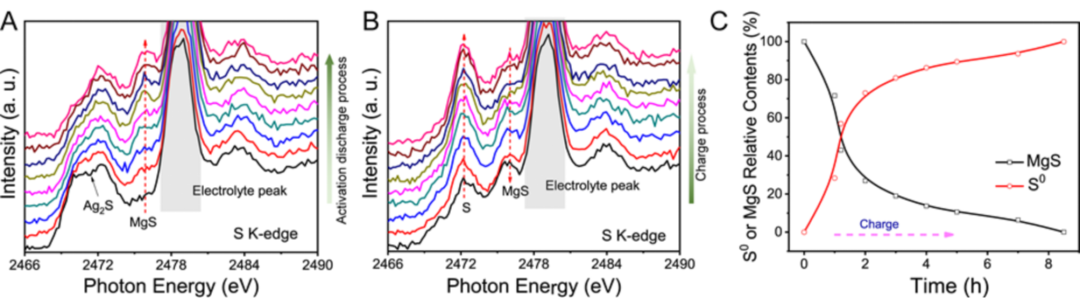
图3 (A)活化过程中S K-edge 原位XAS谱;(B)第1次充电过程中S K-edge原位XAS谱;(C)充电过程中S0和MgS的含量变化。
3. 反应机理结合原位XRD和原位XAS表征结果,研究人员提出如下反应机制(如图4所示)。活化过程:i-Ag2S + Mg2+ + 2e- → MgS + 2Ag (Reaction 1)充电过程:xMgS – 2(x-1)e-  MgSx + (x-1)Mg2+ (Reaction 2)MgSx + (z+1)Ag + zCl- - (z+2)e- → Mg2+ + xS + zAgCl@Ag (Reaction 3)放电过程:Mg2+ +xS + zAgCl@Ag + (z+2)e- → MgSx + (z+1)Ag + zCl- (Reaction 4)MgSx + (x-1) Mg2++ 2(x-1)e-
MgSx + (x-1)Mg2+ (Reaction 2)MgSx + (z+1)Ag + zCl- - (z+2)e- → Mg2+ + xS + zAgCl@Ag (Reaction 3)放电过程:Mg2+ +xS + zAgCl@Ag + (z+2)e- → MgSx + (z+1)Ag + zCl- (Reaction 4)MgSx + (x-1) Mg2++ 2(x-1)e-  xMgS (Reaction 5)
xMgS (Reaction 5)
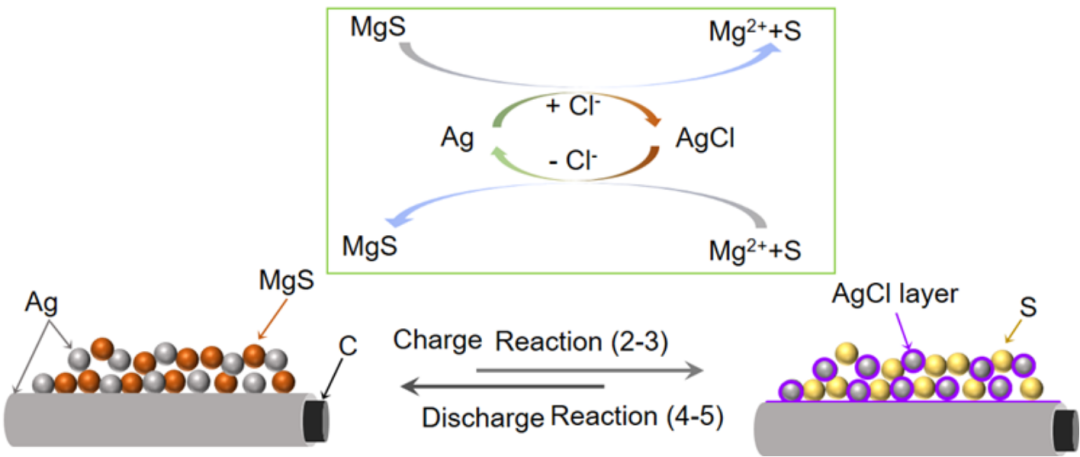
图4 Mg/Ag@S电池反应示意图
【结论】银催化剂与含氯的电解质结合使用实现了可逆功能化催化,极大地提高了 Mg/S 电池的性能。原位XRD 和原位 XAS 研究表明S正极中存在Ag和AgCl之间的可逆转化;AgCl保护层提高了S利用率,而Ag催化了MgS分解。这种可逆的功能切换是镁硫电池性能提升的关键,这一发现将会促进研究人员对S正极中高效催化剂的研究。
Yan Xu, Yuxing Zhao, Shuyang Zhao, Jifang Zhang, Jia Li, Jinghua Guo, Yuegang Zhang, Reversible Function Switching of Ag Catalyst in Mg/S Battery with Chloride-Containing Electrolyte, Energy Storage Mater., 2021https://doi.org/10.1016/j.ensm.2021.08.009
